11.10.2003
Blauwdruk voor toekomstige anabolen
Glass' artikel gaat over de spiercel en wat daar op moleculair niveau gebeurt als de cel hypertrofieert of atrofieert. Het gaat dus over mechanismen waarop nieuwe middelen kunnen aangrijpen, niet over de middelen zelf.
De reden voor Glass om zijn overzicht te maken zijn de tegenvallende ervaringen met wat op papier de allerbelangrijkste anabole factor is: IGF-1. Niet alleen neutraliseren allerlei bindingseiwitten IGF-1 voordat het zijn werk kan doen, maar tot overmaat van ramp beschikken cellen in praktisch alle weefsels - dus niet alleen spiercellen - receptoren voor IGF-1. IGF-1 laat in al die weefsels nieuwe cellen ontstaan. Daardoor heeft IGF-1 veel bijwerkingen, en kijken onderzoekers naar andere aangrijpingspunten.
Anabole aangrijpingspunten
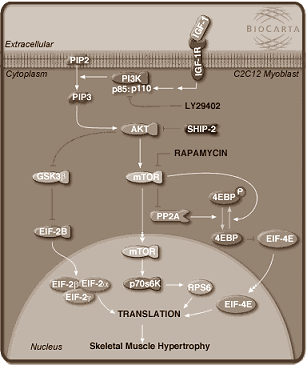
Nadat IGF-1 koppelt aan zijn receptor wordt het eiwitje P13K actief. Gebeurt dat niet, dan doet IGF-1 niets. Lukt het je om de aanmaak van P13K te verhogen, dan groeit de spiercel. P13K zorgt er vervolgens voor dat het eiwit Akt1 fosforgroepen aan allerlei signaalmoleculen gaat plakken waardoor de spiergroei begint.
Akt1 wordt tegengewerkt door SHIP1, SHIP2 en PTEN. Uitschakelen van die eiwitten, bijvoorbeeld door hun genen te wissen, leidt tot hypertrofie. Wetenschappers zijn huiverig voor knoeien met PTEN omdat het uitschakelen van PTEN de kans op kanker verhoogt.
Het aanschakelen van P13K en Akt1 leidt ertoe dat het molecuul mTOR extra fosforgroepen krijgt. Gefosforyleerd mTOR zorgt voor hypertrofie. Het signaalmolecuul wordt niet alleen actief door anabole hormonen hormonen, maar ook door aminozuren. MTOR zorgt ervoor dat het bindingseiwit PHAS-1 alias 4E-BP wordt geremd en het eiwit eIF-4E actief wordt. MTOR schakelt daarnaast het molecuul p70S6K aan.
Middelen die mTOR en p70S6K activeren leiden tot hypertrofie. Dat geldt ook voor middelen die PHAS-1/4E-BP afremmen.
Als Akt1 actief wordt, remt dat het enzym glycogeen-synthase kinase 3 of GSK3. Uitschakelen van dat enzym leidt tot een 'dramatische hypertrofie' in skeletspieren. Het enzym remt de werking van het spieropbouwende eIF-2B. Ook GSK3 is dus een interessant aangrijpingspunt voor anabolica.
Antikatabole aangrijpingspunten
Als spierweefsel afbreekt spelen ubiquitines een sleutelrol. De eiwitjes maken zich vast aan de af te breken eiwitten, en lokken de moleculaire eiwitversnipperaar proteasoom naar de eiwitten.
Het domweg remmen van alle ubiquitines is geen interessante optie, omdat ubiquitines ook virussen en afvalproducten vernietigen. Er zijn enkele honderden ubiquitines bekend, die zich allemaal aan een specifiek af te breken eiwit vastmaken. De genen voor MuRF1 en MAFbx maken ubiquitines die specifiek spierweefsel afbreken. Die genen slaan bijvoorbeeld aan als er glucocorticoidhormonen koppelen aan hun receptoren spiercellen, of spiercellen lange tijd inactief zijn.
MuRF1- en MAFbx-blokkers lijken niet interessant voor sporters. Muizen zonder die genen verliezen minder snel spiermassa dan normale muizen, maar hun spieren zijn niet groter dan normaal.
Slot
Moleculair onderzoek heeft veel aan het licht gebracht over de mechanismen achter hypertrofie, besluit Glass. Hij hoopt dat die kennis leidt tot nieuwe medicijnen met een spierversterkende werking. Nu de vergrijzing toeslaat, en steeds meer mensen kanker krijgen, hebben we die middelen harder nodig dan ooit.
Bron:
Trends Mol Med. 2003 Aug;9(8):344-50.