Het Anabolenboek
Willem Koert
Aede de Groot
Wageningen, 24/2/2007
10. Enzymatische Reacties van Anabole Steroiden
Aede de Groot, Willem Koert
De meeste enzymatische omzettingen die anabole steroiden ondergaan in het lichaam zijn ongewenst. Ze zetten het toegediende anabool immers om in onwerkzame stoffen voordat het zijn werk heeft kunnen doen. Er zijn veel chemische en medische trucs bedacht om die omzettingen te voorkomen. Toediening via een injectie voorkomt bijvoorbeeld omzettingen in de maag, het darmkanaal en de lever. Deze toedieningsvorm was in de hoogtijdagen van het steroidenonderzoek niet populair. Het is nu eenmaal eenvoudiger om een anabool gewoon te slikken. Maar dan moet het wel oraal beschikbaar zijn. Er is veel onderzoek gedaan om dergelijke oraal beschikbare anabolen te ontwikkelen.
We zullen in dit hoofdstuk eerst in algemene zin de omzettingen op een rijtje zetten die enzymen met C-atomen van het steroidskelet van anabolen kunnen uitvoeren. Dit zijn vooral de reacties die optreden met de carbonylgroep op C3, met de hydroxylgroep op C17 en met ring A van het steroid.
Daarna komen ook een aantal enzymatische derivatiseringsreacties van steroiden aan de orde. Derivatiseringsreacties zijn reacties die plaatsvinden met de substituenten die aan het steroidskelet zitten. Vaak hangen de enzymen daar dan een andere groep aan. Bij anabole steroiden zijn vooral de omzettingen van de hydroxylgroepen op C17 en C3 tot sulfaten, glucuroniden en esters van belang.
Cytochroom P450-enzymen
De biosynthese van de geslachtshormonen begint als het enzym cytochroom P450scc de zijketen van cholesterol oxideert. Oxidatie betekent hier het invoeren van zuurstof in de verbinding. Cytochroom P450-enzymen hebben een heemmolecuul nodig als co-enzym. Dit heemmolecuul bevat ijzer - en samen met zuurstof zorgt dat voor oxidatie.
Cytochroom P450-enzymen komen op veel plaatsen in het lichaam voor, en oxideren daar allerlei stoffen. Vooral de lever bevat veel cytochroom P450-enzymen. Cytochroom P450-enzymen zorgen voor het invoeren van zuurstof in organische verbindingen, in de vorm van een hydroxylgroep. Deze hydroxylgroep kan daarna binden met andere stoffen zoals glucuronzuur of sulfaat. Dat maakt de verbinding als geheel meer polair en dus ook oplosbaar in het eveneens polaire water. In deze oplosbare vorm scheiden de nieren en de lever de gemetaboliseerde stoffen uit via respectievelijk de urine of de gal.
Cytochroom P450-enzymen in de lever zijn niet erg specifiek. Ze grijpen aan op een veelheid aan stoffen die met het voedsel binnenkomen en maken die onschadelijk. Cytochroom P450-enzymen die op andere plaatsen in het lichaam hun werk doen zijn vaak specifieker. Ze oxideren maar een enkele verbinding op een specifieke plaats in het molecuul. Sommige cytochroom P450-enzymen kunnen een beperkt aantal sterk op elkaar lijkende stoffen oxideren. We specificeren deze selectieve cytochroom P450-enzymen met een aanvullende code die verwijst naar de reactie die ze katalyseren.
De letters scc in het cholesterol oxiderende cytochroom P450scc betekenen cleavage of cholesterol side chain. Dat geeft aan dat dit enzym de zijketen van cholesterol kan afsplitsen. Dit cytochroom oxideert de zijketen van cholesterol op C20 en C22 door twee OH-groepen in te voeren. Hetzelfde enzym breekt daarna de keten tussen deze twee C-atomen onder vorming van pregnenolon (zie Schema 1).
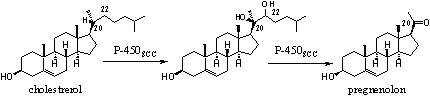
Schema 1
Het enzym cytochroom P45017a katalyseert de invoering van een hydroxylgroep op C17 in een steroid aan de a-kant - de onderkant - van het molecuul. Dit enzym kan dat niet alleen doen in pregnenolon maar ook in het daarop lijkende progesteron (zie Schema 2).
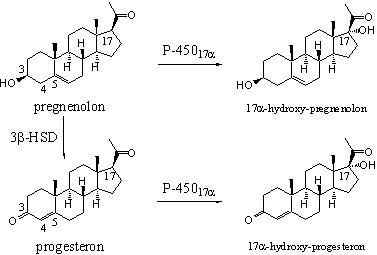
Schema 2
Meerdere cytochroom P450-enzymen zijn betrokken bij de biosynthese van de corticosteroiden. Deze steroiden zijn betrokken bij de stofwisseling van suikers, eiwitten en vetten en bij de mineraal(zout)huishouding van het lichaam. In Schema 3 zien we de invoering van een hydroxylgroep op C21 in progesteron en in 17a-hydroxyprogesteron, die gekatalyseerd wordt door cytochroom P450C21. De invoering van een b-hydroxyl groep op C11 in 11-deoxycorticosteron en 11-deoxycortisol wordt gekatalyseerd door cytochroom P45011b. Beide cytochroom P450-enzymen accepteren dus ook in dit geval beide substraten.
Schema 3
Klik voor grotere afbeelding
Het cytochroom P450aldo katalyseert de oxidatie van de C18-methylgroep tot de carbonylgroep. Een andere naam voor deze functionele groep is aldehydegroep. Die groep is karakteristiek voor aldosteron en geeft ook de naam aan het betreffende enzym. Verderop komen we nog meer cytochroom P450-enzymen tegen.
Oxido-reductase enzymen
In Schema 3 is ook een reactie aangegeven die gekatalyseerd wordt door een enzym dat kortweg 11b-HSD heet. De volledige naam van dit enzym is 11b-hydroxy steroid dehydrogenase. Dat enzym kan zowel oxidaties als reducties katalyseren en hoort bij een grote groep enzymen die oxido-reductases heten.
Dehydrogenasases en oxido-reductases katalyseren oxidaties op een andere manier dan cytochroom P450-enzymen. P450-enzymen voeren een zuurstof atoom (O-atoom) in door oxidatie van een C-H binding. De nieuwe groep wordt dan een hydroxylgroep.
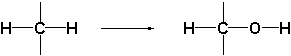
De dehydrogenases en oxido-reductases oxideren de hydroxylgroep verder tot een carbonylgroep door het onttrekken van waterstof. Enzymen die waterstof (hydrogeen) onttrekken aan een verbinding heten dehydrogenases. Deze enzymen gebruiken daarvoor ook een andere hulpstof, een ander co-enzym, dan cytochroom P450-enzymen.
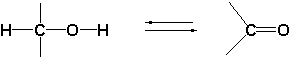
Een tweede kenmerkend verschil tussen cytochroom P450-enzymen en dehydrogenases is dat de reacties van cytochroom-P450-enzymen maar een kant opgaan, terwijl de reacties van dehydrogenases meestal beide kanten op kunnen. Cytochroom P450-enzymen kunnen een hydroxylgroep invoeren, maar kunnen die er niet weer afhalen. Daarom staat in het bovenste reactieschema maar een enkele pijl die slechts een enkele kant opwijst.
Dehydrogenases kunnen een hydroxylgroep oxideren tot een carbonylgroep, maar kunnen die carbonylgroep ook weer reduceren tot een hydroxylgroep. Daarom staat in het onderste reactieschema een dubbele pijl, die aangeeft dat de reactie beide kanten op kan. Het is een evenwichtsreactie. De ligging van het evenwicht is afhankelijk van de omstandigheden. Als de concentratie (de hoeveelheid aanwezige stof) van de hydroxylverbinding hoog is dan wordt deze omgezet in de carbonylverbinding en omgekeerd. Meestal zijn beide verbindingen aanwezig.
Met oxidatie bedoelen we het invoeren van zuurstof (O) in een verbinding of het onttrekken van waterstof (H) aan een verbinding. Reductie is het omgekeerde van oxidatie. Het is het invoeren van waterstof of het onttrekken van zuurstof.
Voor het metabolisme van anabole steroiden zijn vooral de dehydrogenases van belang die de hydroxylgroepen op C3 en C17 kunnen oxideren tot carbonylgroepen en deze omgekeerd weer kunnen reduceren tot de hydroxylgroepen. De volledige naam van 17b-HSD is 17b-hydroxy steroid dehydrogenase of 17b-hydroxy steroid oxido-reductase. De laatste naam geeft de capaciteiten van dit enzym eigenlijk beter weer dan de eerste. Uit die naam blijkt dat het enzym beide functies kan uitoefenen, de oxidatie en de reductie.
Het 17b-HSD reduceert de carbonylgroep op C17 tot een C17-b-hydroxylgroep. Die hydroxylgroep wijst naar boven, het H-atoom naar beneden. Er bestaat ook een 17a-HSD (17a-hydroxy steroid dehydrogenase) en dat doet precies het omgekeerde. 17a-HSD zorgt voor een C17-a-hydroxylgroep aan de onderkant, en een H-atoom aan de bovenkant (zie Schema 4). De 3b-HSD en 3a-HSD enzymen doen hetzelfde, maar dan met de carbonylgroep aan C3.
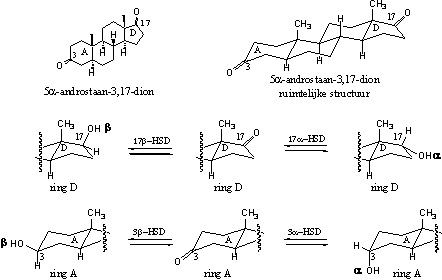
Schema 4
Isomerase-enzymen
Chemici noemen verbindingen die alleen maar van elkaar verschillen in de plaats van een functionele groep, maar verder gelijk zijn, isomeren. Enzymen die de omzetting van het ene isomeer in het andere katalyseren heten isomerases. In de biosynthese van testosteron is een isomerase werkzaam met de naam 3b-hydroxy steroid dehydrogenase/D5-D4-isomerase.
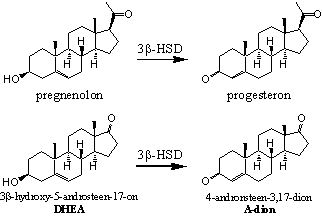
Schema 5
Dit enzym heeft een dubbele functie. Het katalyseert de oxidatie van de hydroxylgroep op C3 tot een carbonylgroep en daarna ook de verschuiving (de isomerisatie) van de dubbele binding van D5 (de C5-C6 positie) naar D4 (de C4-C5 positie). Het enzym kan meerdere substraten, die allemaal een C3-hydroxylgroep en een D5- dubbele binding hebben, omzetten in verbindingen met een C3-carbonylgroep en een D4 dubbele binding (zie Schema 5). Deze reacties gaan allemaal maar een kant op.
Als 3b-HSD zijn werk doet, oxideert het enzym eerst de hydroxylgroep tot een carbonylgroep. Daarna treedt de isomerisatie van de dubbele binding op. Deze isomerisatie verloopt gemakkelijker wanneer er een carbonylgroep op C3 zit. Dat komt omdat structuren waarin afwisselend enkelvoudige en dubbele bindingen voorkomen, zoals O=C-C=C, extra gestabiliseerd zijn en daarom makkelijker worden gevormd.
Reductases
Structuren waarin afwisselend enkelvoudige en dubbele bindingen voorkomen, zoals O=C-C=C, heten geconjugeerde systemen. Ze zijn stabieler dan niet-geconjugeerde structuren, waarin de functionele groepen verder van elkaar zijn verwijderd, en elkaar niet kunnen beinvloeden in hun reacties. Deze geconjugeerde systemen reageren in sommige reacties juist beter. Zo�n reactie is de reductie van de geconjugeerde D4 dubbele binding naar een enkelvoudige binding. Dat is de reactie die moet plaatsvinden voor de omzetting van testosteron in dihydrotestosteron.
Net als bij de dehydrogenases kan ook hier de reductie, de invoering van H-atomen, aan de onderkant of aan de bovenkant op positie C5 van het molecuul plaatsvinden. Die reducties zijn het werk van respectievelijk 5a- en 5b-reductase (zie Schema 6). Het enzym 5a-reductase of kortweg 5AR voert een H-atoom in op de 5a-plaats van testosteron tijdens de biosynthese van dihydrotestosteron. Ook deze enzymatische reactie verloopt maar een kant op. Het enzym 5AR kan niet weer een dubbele binding invoeren.
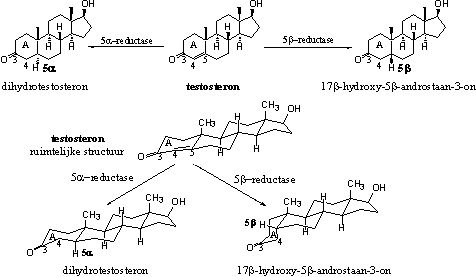
Schema 6
Wanneer 5b-reductase het H-atoom op de 5b-plaats invoert ontstaat een verbinding met een andere vorm in het linkerdeel van het molecuul. Deze verbinding is niet biologisch actief.
Aromatase
De vrouwelijke geslachtshormonen estron en estradiol hebben een bijzondere ring A. Hun A-ring is aromatisch. Deze naam heeft in de verte inderdaad iets met aroma te maken. Eenvoudige verbindingen met eenzelfde soort structuur als in ring A van estron en estradiol, hebben een sterke geur (aroma). Voorbeelden van zulke sterk geurende aromatische verbindingen zijn benzeen en tolueen (zie Schema 7). Tolueen is een gangbaar oplosmiddel in de chemie, benzeen komt regelmatig op ongunstige wijze in het nieuws als milieu-verontreinigende en kankerverwekkende stof.
In de chemie noemen we verbindingen aromatisch als ze een ring van zes C-atomen hebben, met daarin afwisselend enkele en dubbele bindingen. Dit soort verbindingen is extra stabiel en dat maakt hun vorming gemakkelijker. Het enzym aromatase zorgt voor de vorming van zo�n aromatische ring A in estron en estradiol.
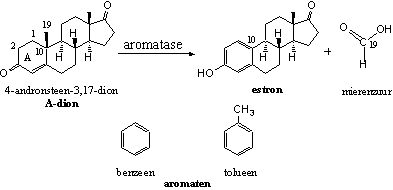
Schema 7
De uitgangsstof in de biosynthese van estron of estradiol is A-dion of testosteron. Voor de aromatisering van ring A is het noodzakelijk dat de C19-methylgroep weg gaat. Koolstof heeft maar vier bindingsmogeljkheden, en in A-dion en testosteron zijn die voor C10 allemaal bezet. Een extra dubbele binding tussen C1 en C10 is pas mogelijk als de C19-methylgroep aan C10 verdwijnt. Een complex van cytochroom P450-enzymen met de code P450aromatase of kortweg aromatase voert deze reactie uit. Dit enzym oxideert eerst de C19-methylgroep tot een hydroxylgroep en daarna tot een carbonylgroep. Die carbonylgroep splitst af in de vorm van mierenzuur, tegelijkertijd met een H-atoom van C1.
Het voorkomen van aromatisering, ofwel het voorkomen van de vorming van estrogenen, is belangrijk voor de behandeling van oestrogeen-afhankelijke kankers. Om die reden hebben biochemici veel onderzoek gedaan naar aromatase-remmers. Ook voor bodybuilders is aromatisering van anabole steroiden vervelend, omdat de daardoor gevormde estrogenen de vorming van borsten bij mannen (gynaecomastia) als bijwerking hebben. Een aromatase-remmer kan echter ook dit probleem oplossen.
Bovenstaande enzymatische reacties hebben allemaal een verandering aan de C-atomen van het skelet van het steroid tot gevolg. In het begin van dit hoofdstuk is al opgemerkt dat er ook een aantal belangrijke enzymatische reacties zijn, die niet met het skelet, maar met de substituenten plaatsvinden. Deze reacties treden vooral op met hydroxylgroepen op C3 en C17. Sulfatase-, glucuronidase- en esterase-enzymen zetten deze hydroxylgroepen respectievelijk om in sulfaten, glucuroniden en esters.
Sulfatases
Allerlei koolstofverbindingen moeten, direct of nadat ze hun functie hebben vervuld, uit het lichaam verwijderd worden. Steroiden bevatten veel apolaire CH2- en CH3-groepen en weinig polaire OH-groepen of C=O-groepen. Steroiden zijn dus overwegend apolair van karakter en daarom zijn ze slecht of niet-oplosbaar in het polaire waterige milieu van bloed, darm en urine. Die oplosbaarheid in water moet verbeteren om uitscheiding via de nieren in de urine mogelijk te maken. Dat gebeurt door sterk polaire groepen, die goed in water oplossen, aan het steroid te hangen. Daardoor verbetert de oplosbaarheid van het hele molecuul in water. Het lichaam gebruikt hiervoor sulfaatgroepen, afgeleid van zwavelzuur, en glucuronzuurgroepen, afgeleid van de suiker glucose.
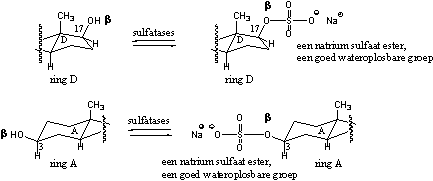
Schema 8
Een zwavelzuurderivaat reageert met de hydroxylgroepen in het steroid tot sulfaat-esters. Die reactie wordt gekatalyseerd door sulfatases. Sulfatases zetten vooral de 3b-OH-groepen en de 17b-OH-groepen om in sulfaten. De sulfaten kunnen ook weer gehydrolyseerd worden tot de oorspronkelijke OH-groepen. (zie Schema 8).
Glucuronidases
Glucuroniden zijn metabole producten van steroiden. Het lichaam maakt ook hier deze derivaten om de apolaire steroiden beter oplosbaar te maken in water. Glucuroniden vormen een aparte groep binnen de grote groep van de glycosiden. Glycosiden zijn producten die via een glycoside-binding gebonden zijn aan een suikermolecuul. Ze komen veel voor in de natuur (zie Schema 9).
De algemene naam van de binding in glycosiden is acetaal. Een glycoside is een acetaal van een suiker. Acetalen zijn het belangrijkste type binding in suikers. Hun biosynthese wordt gekatalyseerd door glycosidases. We zullen acetalen in het vervolg nog tegenkomen. Bedrijven brengen een aantal anabole steroiden als acetaal op de markt.
Glucuroniden zijn dus glycosiden of acetalen van glucuronzuur. Glucuronzuur ontstaat door oxidatie van de CH2OH groep (C6) van de suiker glucose tot een carbonzuur-(COOH)-groep. De reactie van de hydroxylgroep aan C1 van het glucuronzuur met een hydroxylgroep van het steroid geeft daarna het glucuronide (zie Schema 9).
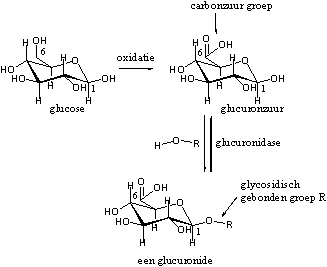
Schema 9
De vorming van glucuroniden wordt gekatalyseerd door een subgroep van de glycosidases, de glucuronidases. Dit zijn enzymen die alleen maar omzettingen met glucuronzuur katalyseren. De reactie is een evenwicht. Het glucuronidase kan het glucuronide ook weer hydroliseren tot het steroid en glucuronzuur.
De plaats waar glucuronidases bij voorkeur actief zijn, is de 3a-hydroxylgroep aan C3 in steroiden. Sulfaten hebben daarentegen een voorkeur voor de 3b-hydroxylgroep. Ook de 17b-hydroxylgroep wordt vaak omgezet in een glucuronide (zie Schema 10).
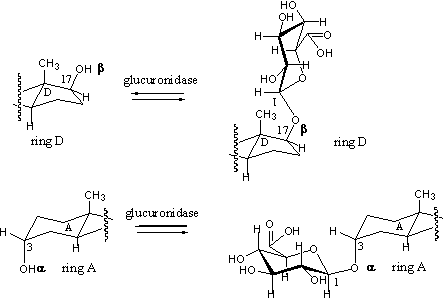
Schema 10
Esterases
Esterases zijn enzymen die bijna overal in het lichaam voorkomen. Ze katalyseren de vorming en de hydrolyse van esters. Esters ontstaan door een reactie van een carbonzuur met een alcohol, een reactie waarbij water vrijkomt. Een eenvoudig voorbeeld is de vorming van de ester ethylacetaat door de reactie van azijnzuur met ethanol (gewone alcohol). Omgekeerd kunnen esters weer met water hydrolyseren tot een carbonzuur en een alcohol. Het is een evenwichtsreactie (zie Schema 11).

Schema 11
In de natuur komen steroidhormonen niet in het lichaam voor in de vorm van esters. Het lichaam zal anabole steroiden ook niet omzetten in esters van carbonzuren. Toch willen we hier de esterases noemen omdat die enzymen wel de esters van anabole steroiden kunnen hydrolyseren. Veel commerciele injecteerbare anabole steroiden zijn esters.
De vetten in onze voeding zijn esters van de drievoudige alcohol glycerol (een triol). Die triesters vormen een grote varieteit aan vetten (zie Schema 12).
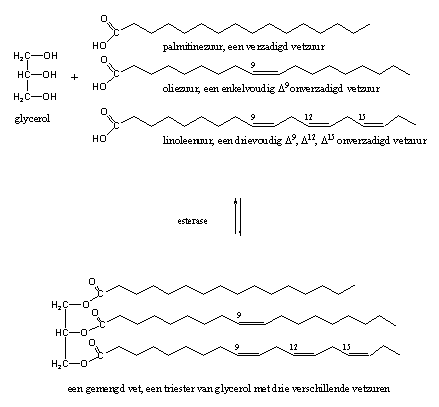
Schema 12
Esterases hydroliseren esters, ook die van steroiden. Dit betekent dat de enzymen de ester van het steroid weer splitsen in een los carbonzuur en een hydroxylgroep die aan het steroid zit. Dit betekent dat we anabole steroiden in de vorm van esters door middel van injectie in het lichaam kunnen brengen. De esterases hydrolyseren die esters langzaam en maken zo het werkzame anabool vrij (zie Schema 13).
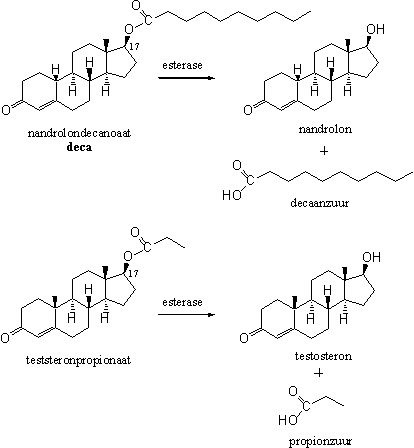
Schema 13
Voorbeelden zoals deca en testosteronpropionaat zijn algemeen bekend, maar er zijn vele variaties op dit thema op de markt. Er zijn ook veel variatiemogelijkheden, want in principe kunnen chemici elk carbonzuur aan elke hydroxylgroep van het steroid binden. Randvoorwaarden zoals vetoplosbaarheid, transportmogelijkheden en kwetsbaarheid voor metabole omzettingen bepalen de juiste combinatie.
|
|