Het Anabolenboek
Willem Koert
Aede de Groot
Wageningen, 15/4/2007
13. Chemische Trucs tegen Ongewenste Metabole Omzettingen van Anabole Steroiden
Aede de Groot, Willem Koert
Dit hoofdstuk gaat over de pogingen van chemici om ongewenste enzymatische omzettingen van anabole steroiden te voorkomen en tegelijkertijd hun werking te verbeteren. Veel anabolen lijken op de natuurlijke steroiden in ons lichaam en kunnen daarom vaak ook door dezelfde enzymen omgezet worden die bij de synthese van de natuurlijke steroiden zijn betrokken. Daarover gaan hoofdstuk 10 en hoofdstuk 11. In hoofdstuk 12 hebben we echter gezien dat er chemische of sterische trucs zijn om die omzettingen lastiger te maken. We zullen ze in dit hoofdstuk per groep enzymen behandelen.
Cytochroom P450-enzymen
Cytochroom P450-enzymen kunnen samen met zuurstof hydroxylgroepen invoeren in het steroid. Dit is vaak een eerste noodzakelijke stap voor de verwijdering van het steroid uit het lichaam. Enzymen zetten de ingevoerde hydroxylgroepen om in glucuronaten of sulfaten. Daardoor neemt de polariteit van het molecuul toe, en daarmee zijn oplosbaarheid in water. De nieren scheiden via de urine de opgeloste steroiden uit.
In het lichaam kunnen enzymen hydroxylgroepen invoeren bij steroiden op C6 en C16 - en natuurlijk bij de plaatsen die tijdens de biosynthese van de natuurlijke steroiden een hydroxylgroep krijgen. In zeldzame gevallen krijgen steroiden ook hydroxylgroepen op C12, C18 en C19.
De oxidatie op C6 ligt voor de hand. De nabijheid van de dubbele binding maakt hem reactiever dan andere plaatsen.
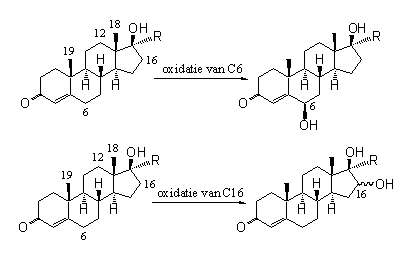
Schema 1
Als de meest voor de hand liggende plaatsen in het steroid niet beschikbaar zijn voor reactie, dan vinden soms reacties plaats op minder voor de hand liggende plaatsen. Soms ook vinden waarschijnlijke reacties niet plaats. Dat gebeurt als het steroid al uit het lichaam verwijderd is voordat een reactie kan optreden. Dit laatste is mogelijk als het steroid al een paar hydroxylgroepen heeft.
Het is niet zinvol om te proberen cytochroom P450-enzymen te remmen. Deze enzymen zijn zo alom aanwezig - en zo belangrijk - voor de bedrijfsvoering van het lichaam dat het niet verstandig is daaraan te beginnen.
Oxido-reductase-enzymen voor C17
De carbonylgroep op C3 en de hydroxylgroep op C17 zijn noodzakelijk voor een goede interactie tussen het anabole steroid en de androgeenreceptor. Elke enzymatische omzetting van deze groepen is ongewenst. In het voorbeeld in hoofdstuk 12 is uitgelegd dat een 17a-methylgroep het probleem van de voortijdige oxidatie van de 17b-hydroxylgroep verhelpt (zie Schema 2) en steroiden oraal beschikbaar maakt. Chemici hebben lange tijd gedacht dat nog grotere groepen op deze plaats een goede interactie met de receptor zouden schaden, maar ervaringen en berekeningen met THG en norboleton hebben aangetoond dat dit niet altijd het geval is.
We hebben eerder al gewaarschuwd voor mogelijk schadelijke neveneffecten van 17a-methyl anabolen. Artsen ontraden het gebruik van deze middelen, tenzij uitvoerige tests hebben vastgesteld dat deze neveneffecten afwezig zijn.
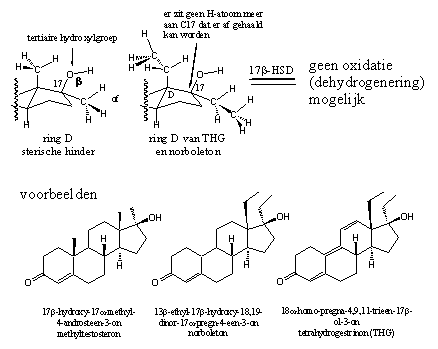
Schema 2
Oxido-reductase-enzymen voor C3
Het is lastiger de carbonylgroep op C3 te behoeden voor een reductieen te voorkomen dat die omzet in een a- of b-hydroxylgroep. In hoofdstuk 2 hebben we opgemerkt dat een dubbele C=C binding vlak is. Dat geldt ook voor een dubbele C=O binding. Dat betekent dat een carbonylgroep van boven en van onderen goed toegankelijk is voor reacties. Voor een reductie in het lichaam moeten enzymen H-atomen toevoegen. Daarvoor hebben ze bij de carbonylgroep op C3 dus alle ruimte. Aangezien alle vier bindingsmogelijkheden van C3 al in gebruik zijn, is er geen mogelijkheid om de carbonylgroep te beschermen door meer groepen aan het betreffende C3-atoom te hangen die hem door sterische hinder zouden beschermen.
Een grotere sterische hinder voor reductie is echter wel mogelijk door extra groepen te zetten aan de C-atomen naast de carbonylgroep, dus op C2 en/of C4. Dat hebben chemici ook gedaan, zoals blijkt uit de voorbeelden in Schema 3. In drostanolon en stenbolon zit een methylgroep op C2, in clostebol zorgt het chlooratoom op C4 voor sterische hinder. In stenbolon zijn daarbij nog een D1-dubbele binding en is in clostebol een D4-dubbele binding aanwezig. De dubbele bindingen zorgen voor aanvullende bescherming van de carbonylgroep tegen reductie.
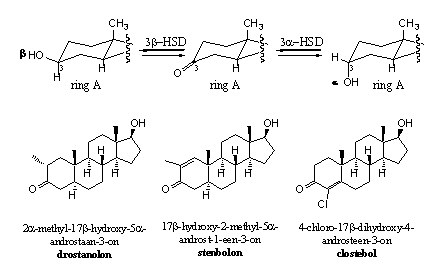
Schema 3
Het reduceren van de carbonylgroep is ook te bemoeilijken door de carbonylgroep zelf stabieler te maken. Dat kan door de carbonylgroep deel uit te laten maken van een geconjugeerd systeem met afwisselend enkele en dubbele bindingen (C=C-C=O). Zulke systemen zijn stabieler dan systemen waarin deze afwisseling niet aanwezig is. Daarom zien we die systemen in veel anabole steroiden terug – bijvoorbeeld tussen C1 en C2 (D1), tussen C4 en C5 (D4) of allebei (zie Schema 3 en Figuur 1). Ook uitgebreidere geconjugeerde systemen komen voor, zoals in trenbolon en THG (zie Schema 2).
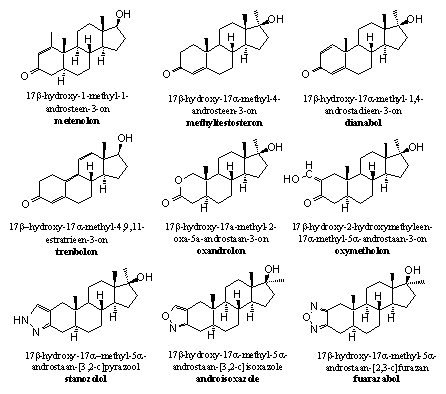
Figuur 1
Een derde mogelijkheid is het aanbrengen van een geheel ander, stabieler structuur element op of rond C3, met of zonder behoud van de carbonylgroep. Voorbeelden hiervan zijn oxandrolon, oxymetholon en stanozolol (zie Figuur 1).
In oxandrolon is de C3-carbonylgroep onderdeel van een cyclische ester. Chemici noemen zo'n verbinding een lacton. Het O-atoom in de ring stabiliseert de carbonylgroep en vermindert dus de gevoeligheid voor reductie.
In oxymetholon zien we dat de carbonylgroep in een geconjugeerde positie zit, nu met een dubbele binding naar buiten aan de ring op C2. De hydroxylgroep aan die dubbele binding zorgt heeft een aanvullend stabiliserend effect.
In stanozolol, androisoxazool en furazabol is de carbonylgroep vervangen door een kleine ring. Deze heterocyclische ring is aromatisch en daardoor extra gestabiliseerd. De aanduiding hetero betekent dat een aantal C-atomen in die ring zijn vervangen door andere atomen, in deze gevallen dus door N- en O-atomen. Het onderste N-atoom in deze ringen is een waterstofbrug-acceptor en vervult waarschijnlijk die functie in plaats van de carbonylgroep.
De dubbele bindingen en de andere veranderingen in de structuur van steroiden zorgen ook voor vormveranderingen en voor andere interactiemogelijkheden. De hoop is natuurlijk dat dit nadelig is voor omzetting door het enzym en tegelijk voordelig voor de interactie met de androgeenreceptor. Dit is niet bij voorbaat onmogelijk. Het enzym en de receptor zijn twee verschillende eiwitten. We zien dit effect bijvoorbeeld optreden bij THG en trenbolon.
Reductases
De reductie van de D4-dubbele binding gaat makkelijker als deze dubbele binding geconjugeerd zit met de carbonylgroep op C3. Eerder is opgemerkt dat die geconjugeerde positie de carbonylgroep juist stabieler maakt, en dat is ook zo. Voor de dubbele binding geldt echter het omgekeerde. Die wordt juist kwetsbaarder voor reductie door de nabijheid van een carbonylgroep. Het gaat een beetje ver om daar op in te gaan.
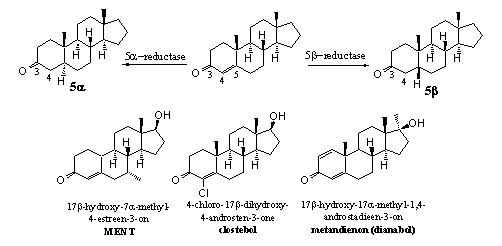
Schema 4
De reductie van de D4-dubbele binding kan vanaf de onderkant of vanaf de bovenkant van het molecuul plaatsvinden. Daardoor ontstaan respectievelijk de 5a- en de 5b-steroiden. Het aanbrengen van extra substituenten, zoals een 7a-methylgroep in bolasteron en MENT, kan de werking van 5AR verhinderen. Methylgroepen aan de onderkant van het molecuul hinderen de nadering van het co-enzym dat de waterstof aan de onderkant moet afleveren.
Ook de invoering van een chlooratoom aan de dubbele binding zoals in clostebol maakt de reductie van de dubbele binding lastiger. Dit is niet alleen een gevolg van sterische hinder, maar ook van de stabiliserende interactie tussen het chlooratoom en de dubbele binding.
De invoering van een extra dubbele binding tussen C1 en C2, zoals in dianabol, blokkeert de reductie van de dubbele binding tussen C4 en C5. De reden hiervoor is niet geheel duidelijk. Het kan zijn dat de verandering van de vorm van het molecuul tot gevolg heeft dat het niet meer past in de reactieholte van het reducerende enzym. Een andere reden kan zijn dat de activerende werking van de carbonylgroep voor de reductie nu verdeeld is over twee dubbele bindingen en daardoor niet meer voldoende is om reductie op D4 nog te laten plaatsvinden.
Door reductie van de D4-dubbele binding in testosteron door het enzym 5AR ontstaat in sommige weefsels dihydrotestosteron. Dat heeft androgene neveneffecten. Als de reductie van de D4-dubbele binding in testosteron plaatsvindt door een 5b-reductase ontstaat het inactieve 5b-dihydrotestosteron.
Het is niet altijd bekend of de verhouding tussen anabole en androgene activiteit verandert als enzymen de D4-dubbele binding reduceren in synthetische anabole steroiden. Er zijn ook een aantal anabole steroiden bekend waarin die D4-dubbele binding sowieso niet aanwezig is. Wat voor testosteron en dihydrotestosteron geldt, hoeft dus niet voor andere anabole steroiden te gelden. We hebben al eerder opgemerkt dat elke verandering in de structuur van het anabool zijn eigen gevolgen kan hebben voor de fysiologische activiteit. Als je die gevolgen wilt weten, moet je die voor elk anabool afzonderlijk uitzoeken door ze uitvoerig te testen.
Glucuronidases en sulfatases
Glucuronidases en sulfatases hebben we beschreven in de schema’s 11 en 12 van hoofdstuk 10. Deze enzymen katalyseren vooral reacties van de hydroxylgroepen op C3 en C17. Ze zetten deze hydroxylgroepen om in glucuroniden of sulfaatesters. Daardoor worden de steroiden polairder en beter oplosbaar in water. Dit zijn dus in principe ongewenste reacties, want ze verminderen de concentratie van werkzame stoffen in het lichaam.
Sterische hinder is nadelig voor de reacties van glucuronidases en sulfatases. Die grotere sterische hinder komt voor de C17-hydroxylgroep vooral van een 17a-methyl of -ethylgroep. Een C13-ethylgroep kan voor nog meer sterische hinder zorgen.
Glucuronidases en sulfatases zetten alleen hydroxylgroepen om in glucuroniden of sulfaten. Met de carbonylgroep op C3 kunnen ze niets. Maar als andere enzymen die carbonylgroep reduceren tot een hydroxylgroep kunnen glucuronidases en sulfatases die hydroxylgroep weer wel omzetten in een glucuronide of sulfaat. We moeten deze reductie dus lastiger maken. Hoe, dat hebben we hierboven uitgelegd (zie Schema 4).
Esterases
Esterases katalyseren meestal reacties die bij anabole steroiden gewenst zijn. Steroiden worden vaak toegediend in de vorm van esters. Dan is het de bedoeling dat die esters langzaam hydrolyseren zodat het werkzame anabole steroid vrijkomt. Het zijn de overal in het lichaam aanwezige esterases die daarvoor zorgen.
|
|